
[Source: Wikimedia]
Andressa Bonafe e Charles Goulding entrevistam um pesquisador líder para aprender mais sobre o estado da bioimpressão.
Nós da R&D Tax Savers temos acompanhado com entusiasmo os desenvolvimentos relativos à bioimpressão 3D ao redor do mundo.
Recentemente, tomamos conhecimento do impressionante trabalho realizado por pesquisadores brasileiros que criaram um protocolo para a impressão 3D de células cerebrais. Curiosos para saber mais sobre o perfil e trajetória dos envolvidos nessa iniciativa, realizamos uma entrevista com a Bruna Alice Gomes de Melo, primeira autora do artigo publicado no Journal of Visualized Experiments (JoVE), na área de bioengenharia, em julho de 2021. Ela nos deu sua perspectiva sobre o cenário atual da bioimpressão 3D e nos contou um pouco sobre alguns projetos nos quais esteve envolvida.
Obrigada por aceitar nosso convite. Poderia nos contar um pouco da sua trajetória de pesquisadora, como se envolveu com a bioimpressão 3D e por que escolheu se especializar nesta técnica?
Cursei licenciatura em química na UNICAMP e fiz mestrado e doutorado em engenharia química. Meu mestrado foi focado em nanopartículas, tema que estava em alta na época
e sobre o qual realizei minha pesquisa de iniciação científica. Já no doutorado, minha orientadora tinha uma linha de pesquisa em medicina regenerativa, área que me interessava. Como consequência, comecei a estudar mais sobre células, biomateriais e técnicas de biofabricação, os três pilares da bioengenharia.
Durante o doutorado eu recebi uma bolsa FAPESP, que me deu a oportunidade de realizar um estágio no exterior. Trabalhei durante nove meses em um laboratório de bioengenharia na Harvard Medical School, sob orientação da Professora Dra. Su Ryon Shin. O grupo de pesquisadores era interdisciplinar, envolvendo pessoas da química, física, medicina e engenharia mecânica. De maneira geral, o laboratório era bastante forte em bioimpressão 3D, técnica que esteve presente em vários dos projetos nos quais me envolvi e que eventualmente resultaram em publicações.
Essa experiência com bioimpressão 3D e medicina regenerativa me levou a realizar um pós-doutorado na UNIFESP, em um laboratório de neurobiologia molecular. A Professora Dra. Marimélia Porcionatto buscava implementar uma equipe mais multidisciplinar que desenvolvesse projetos envolvendo bioimpressão 3D. Com essa missão, submeti um pedido de financiamento à FAPESP que permitiu a aquisição de uma impressora da 3DBS, startup brasileira. Posteriormente, outro financiamento permitiu a compra de uma impressora maior e materiais que viabilizaram um projeto envolvendo células neurais.
Durante toda essa trajetória, meu interesse nunca foi um tecido específico e sim as técnicas de fabricação e bioengenharia. Já trabalhei com células de cartilagem, osso, células cardíacas, tecidos neurais, etc.
Quais você considera serem as maiores vantagens da bioimpressão 3D comparada a outros métodos de fabricação?
A bioimpressão 3D permite criar estruturas complexas, mimetizando tecidos que compõe o organismo humano. Através da bioengenharia essa técnica permite a realização de estudos in vitro, com células vivas, que seriam uma etapa anterior aos modelos animais. Isso é importante porque leva à redução do número de animais envolvidos nas pesquisas. A partir da bioimpressão 3D, temos recursos para avaliar mais precisamente a atuação de medicamentos, vacinas, vírus, etc. Esses modelos são superiores às alternativas 2D, nos quais células são cultivadas em placas, já que os tecidos no organismo humano são tridimensionais. A proximidade morfológica é uma grande vantagem. Mesmo se comparada a outros métodos de produção de estruturas 3D, como a utilização de moldes, a bioimpressão permite a criação de modelos mais complexos, com diferentes combinações de células e biomateriais, o que é possível, por exemplo, por meio da utilização de mais de um bico extrusor. Essa vantagem nos dá a perspectiva de criarmos tecidos diversos e, um dia, até mesmo órgãos para implantes.
Você mencionou seu interesse no método de fabricação em si. Isso envolve a pesquisa de biomateriais?
Sim,um aspecto importante da pesquisa envolvendo bioimpressão 3D é a utilização de biomateriais. Mais especificamente, falamos de polímeros e, em sua maioria, polímeros naturais, que estão presentes no organismo humano, como o colágeno. São utilizados também o ácido hialurônico, a gelatina (colágeno hidrolisado) e até mesmo alguns polímeros sintéticos. No geral, são polímeros mais macios e hidratados, com exceção de casos envolvendo ossos ou próteses, que exigem materiais rígidos como a cerâmica. A diferença da bioimpressão se comparada à impressão 3D tradicional é que os materiais não são submetidos a condições tão severas, envolvendo altas temperaturas. Porém, são necessários estudos detalhados das propriedades dos materiais para determinar sua capacidade de mimetizar os tecidos de interesse. Por exemplo, nos projetos em que participei, queríamos determinar se a combinação de colágeno, gelatina e fibrina seria comparável à mecânica de tecidos cerebrais.
Nos últimos anos, você esteve envolvida em pesquisas muito interessantes e diversas. Poderia nos dar uma visão geral do papel da bioimpressão em alguns desses projetos?
Durante meu período em Harvard, trabalhei com células-tronco mesenquimais e cartilagem. Cartilagem é uma área interessante, porque é um tecido que se desgasta com a idade e não se regenera. Trata-se também de um tecido de menor complexidade, se comparado, por exemplo, aos tecidos neurais. Mesmo assim, o estudo dos materiais foi fundamental para criar um ambiente adequado, que se assemelhasse à cartilagem no que diz respeito à rigidez, mas, ao mesmo tempo, permitisse que as células-tronco mesenquimais se adaptassem e eventualmente se diferenciassem em condrócitos, que são as células da cartilagem. Primeiramente, utilizamos um molde para criar o tecido rígido. Em seguida, misturamos as células-tronco num material mais macio e, com a bioimpressora, imprimimos essa combinação dentro do material rígido. Essa técnica nos permitiu depositar as células na direção e disposição que queríamos. Conseguimos assim um tecido vivo, com a rigidez da cartilagem, mas que contava com um material mais brando ao redor das células, de forma que elas se diferenciaram em condrócitos e expressaram ali seus genes, demonstrando um comportamento similar ao da cartilagem. Esse trabalho foi publicado na revista Advanced Functional Materials.
Mais recentemente, no pós-doutorado, fiz diversos estudos de biomateriais para identificar as combinações e designs de bioimpressão que seriam mais adequados para mimetizar o tecido cerebral. Foram pesquisas preliminares que servirão de base para futuros trabalhos focados em doenças neurodegenerativas.
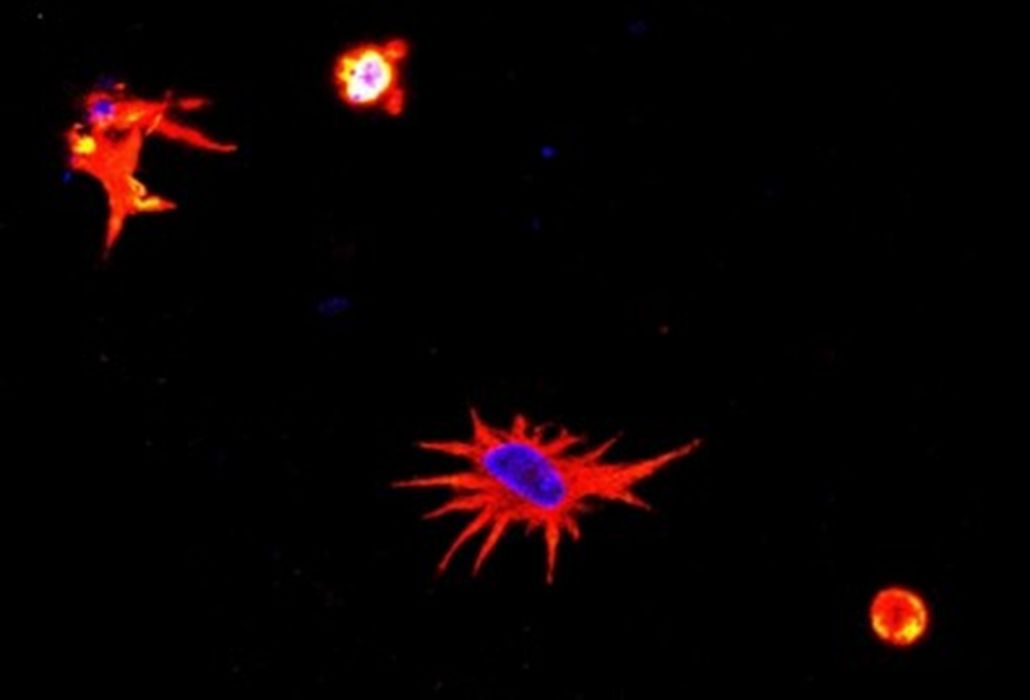
Outro projeto interessante foi o desenvolvimento de um modelo para avaliar os efeitos do SARS-CoV-2 sobre as células neurais. Para construir esse modelo, misturamos astrócitos e neurônios, que são as principais células do tecido neural. Primeiro, realizamos a bioimpressão 3D com os astrócitos, que são mais resistentes, e depois adicionamos os neurônios. Essas células se conectaram e demonstraram reconhecer o ambiente em que estavam como um tecido neural. A partir disso, nosso objetivo era observar o comportamento das células na presença do vírus. Por exemplo, queríamos verificar se haveria expressão de proteínas inflamatórias, se a morfologia das células sofreria mudanças, etc. Outro aspecto interessante do projeto é que usamos células animais e, por isso, tivemos que adaptar o vírus humano para camundongos. Esse projeto, também financiado pela FAPESP, resultou na publicação de um artigo na revista Advanced Biology.
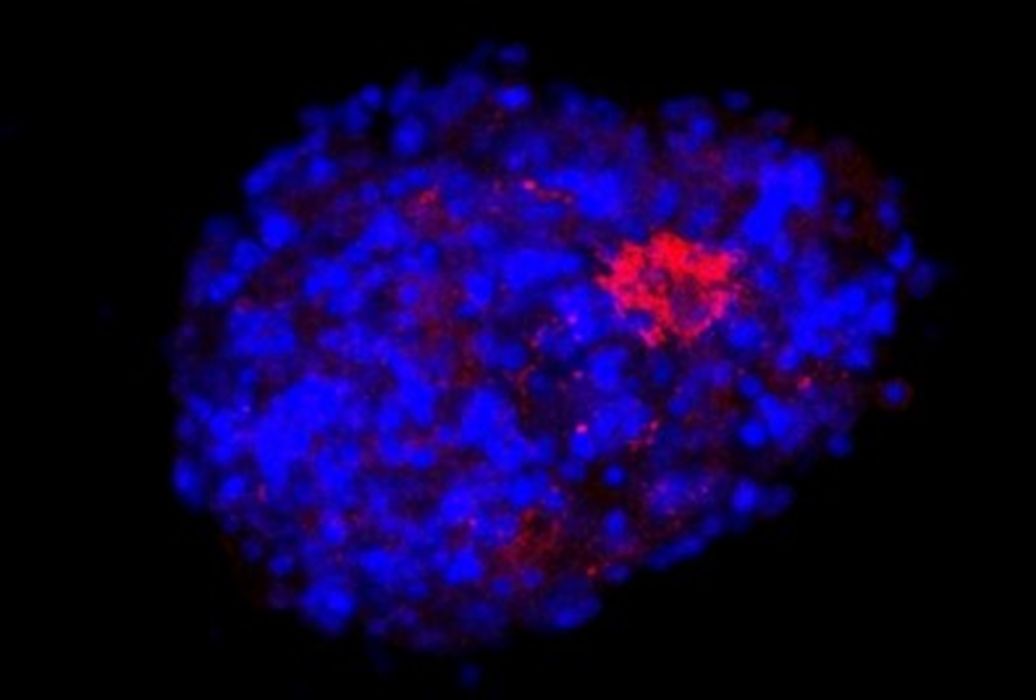
Atualmente, além de trabalhar na iniciativa privada, na startup Nanobioplus, com pesquisa e desenvolvimento de produtos envolvendo biomateriais, sou colaboradora do Shin Lab, da Harvard Medical School, além de ser pesquisadora participante de um grande projeto interdisciplinar que envolve pesquisadores de diversas áreas em todo o país, o Model3D, que é parte do programa Institutos Nacionais de Ciência e Tecnologia. A ideia principal é usar modelos de organoides para estudar doenças crônicas não transmissíveis, como as doenças neurodegenerativas, doenças do neurodesenvolvimento e câncer. A iniciativa conta com um financiamento de mais de R$5,5 milhões e certamente utilizará técnicas de bioimpressão 3D para atingir seus objetivos.
Pensando no futuro da bioimpressão 3D, quais seriam os principais desafios e as áreas que você destacaria como mais promissoras?
Acredito que o principal desafio é desenvolver órgãos funcionais. Na maioria dos casos são tecidos muito complexos. Além de simular a matriz extra celular utilizando biomateriais, teríamos que combinar diversos tipos de células, construir vasos sanguíneos e linfáticos, etc. Criar órgãos completos e funcionais, adequados para transplante, é maior sonho e o maior desafio de quem trabalha com bioimpressão. Temos progredido em direção a esse objetivo, criando e testando pequenos pedaços de tecidos que eventualmente se encaixarão como quebra-cabeças.
Áreas promissoras a curto prazo seriam a expansão a utilização dos tecidos bioimpressos compostos de biomateriais na regeneração de tecidos e pequenas lesões, além da bioimpressão com células humanas para diagnóstico de doenças, testes de novos medicamentos, tratamentos e vacinas.
